骨肉瘤作为一种具有高度侵袭性的恶性肿瘤,其术后高复发率与骨缺损修复困难构成临床重大挑战。近日,中国科学院海西研究院泉州装备制造研究中心林锦新课题组受贻贝黏附机制启发,通过创新性地将二硫化钼(MoS2)的光热转化特性、聚多巴胺(PDA)的表面修饰功能与磷酸八钙(OCP)的成骨活性相结合,采用3D打印技术成功构建了兼具肿瘤治疗与骨修复双功能的一体化复合支架。该支架不仅展现出规整的多孔结构和适宜的力学性能,更在体内、外实验中表现出显著的光热治疗效果和促成骨分化能力,为实现肿瘤消除及原位骨再生提供全新的一体化微创精准治疗策略。
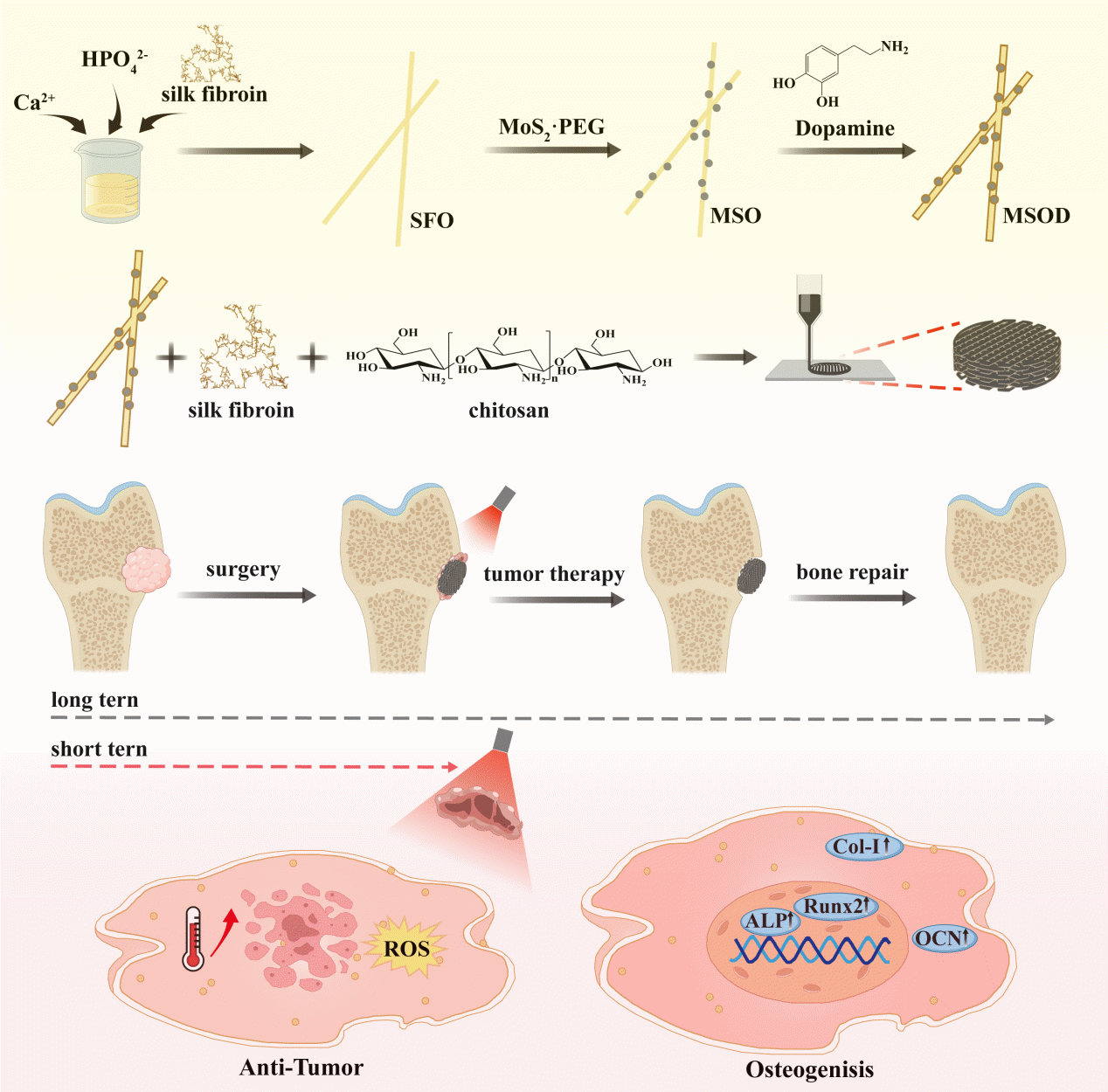
图 1. 3D打印复合支架抗肿瘤/骨修复“综合治疗”的研究示意图。
在这项工作中,复合支架在近红外激光照射下可实现高效的光热转化,通过局部高温和活性氧(ROS)的协同作用有效清除骨肉瘤细胞,体外细胞清除率达90%以上。同时,支架表面的PDA修饰显著改善了材料的亲水性和生物相容性,并通过调控细胞微环境促进成骨细胞黏附、增殖和分化。在大鼠颅骨缺损模型中,该支架展现出卓越的骨再生能力,Micro-CT及组织学分析均证实其能有效促进新骨形成。机制研究表明,该支架通过调节Toll样受体和PPAR信号通路,激活成骨相关基因表达,协同调控骨免疫微环境与骨重塑过程。这种将肿瘤治疗与原位骨修复功能集于一体的创新策略,不仅为骨肉瘤的一体化微创术后治疗提供了新的解决方案,也为多功能生物材料的设计开发提供了重要理论依据和实践参考。

图 2. 3D打印复合支架植入4周、8周和12周的大鼠颅骨CT图像。
相关研究成果以“Mussel-inspired Integrated Functional 3D Printed Scaffolds with Molybdenum Disulfide Nanoflowers for Tumor Therapy and Bone Reconstruction”为题发表于Chemical Engineering Journal期刊上。中国科学院海西研究院泉州装备制造研究中心林锦新研究员、福建医科大学附属口腔医院吴烨教授、福建师范大学卢衍锦副教授为本文通讯作者,李岚博士为本文第一作者。研究工作获得国家自然科学基金、福建省自然科学基金杰青项目、中国福建光电信息科学与技术创新实验室(闽都创新实验室)自主部署项目基金等项目的支持。
论文链接:https://doi.org/10.1016/j.cej.2025.161399
(林锦新课题组供稿)